Chp 06 Alternative Splicing
Molecular Biology of RNA 2nd edition (David Elliott & Michael Ladomery)
자 그럼 이제 Alternative splicing에 대한 기초 공사는 끝났다. 이제 Alternative splicing을 조절하는 regulatory factors, 요인들에 대해 알아보자.
RBP concentration
Alternative splicing은 mRNA의 Splicing code에 결합하는 여러가지 RBP들에 의해서 조절받는다. 따라서 이러한 RBP의 농도에 따라 alternative splicing이 좌우된다는 것은 그리 놀라운 사실은 아닐 것이다. 아래 예시를 간략히 보자.
1. RPL32(yeast ribosomal protein)
 |
RPL32의 대부분은 large rRNA subunit에 결합한다. 그러나 RPL32가 많아지게 되면 excess는 자신의 transcript에 결합해 spliceosome의 결합을 막는다. |
2. Mer2(in yeast meiosis)

Mer2의 5' Splice site는 consensus sequence와 차이가 있어서 U1 snRNP에게 잘 인식되지 않는다. 그러나 Meiosis 때는 ISE에 결합하는 Mer1이 번역되어 U1 snRNP의 5' splice site 인식을 도와 alternative splicing을 촉진한다.
3. TRA(초파리의 성 결정)

초파리는 성별에 따라 splicing 방식이 다르다. 암컷에서만 Sxl RBP가 생성되는데, 생성된 Sxl은 Sxl pre-mRNA에 결합해 positive autoregulation을 진행한다. 또한 암컷은 dosage compensation에 필요한 MSL-2가 필요하지 않기 때문에 대신 TRA pre-mRNA를 생성한다. 생성된 TRA는 double sex pre mRNA 등을 발현시켜 암컷으로의 분화를 돕게 된다. (간략하게만 한 설명이다. 자세한 설명은 책에 있다. 책이 없으면 저런 유감을 표한다. 하지만 당신에게는 구글이 있다.)
Signal transduction pathway
signal transduction pathway가 변하면 protein의 modification, 위치 등이 변할 수 있다. 단언컨데 나비효과.. 같은 거라고 할 수 있지 않을까? (단언컨데와 의문문이 문득 어색하단 생각이 들지만; 마음에 드는 기분이니까 내비둔다.)
이 경우의 예로는 hnRNP A1을 들 수 있다.

hnRNP A1은 스트레스가 없는 상황에서 핵과 세포질 사이에서 steady state를 이루고 있다. 이것이 가능한 이유는 hnRNP A1이 세포질에서 번역되면 M9을 인식하는 단백질에 의해 핵 안으로 수송되기 때문이다.
하지만 스트레스 상황이 되면 MAP kinase와 p38이 활성되어 M9이 인산화 되게 된다. 인산화된 M9은 import 시켜주는 단백질에게 인식되지 못하므로 핵으로 수송되지 못한다. 그 결과 Splicing의 변화가 초래되는 것이다.

Transcription elongation speed
뒤에서 언급하겠지만 전사와 전사 후 가공은 매우 긴밀하게 연결되어 있기 때문에 co-transcriptional pre-mRNA processing이라고 불린다. Splicing은 전사가 진행되는 와중에 시작되기 때문에 전사 진행 속도가 alternative splicing에 영향을 미친다고 할 수 있다. 여기에는 Kinetic coupling model과 Recruitment model이 있는데 오늘은 Kinetic coupling model만 언급하고자 한다. (뒤에건 제대로 이해 못했으니까 ^^;)

RNA polymerase II가 느리게 진행하면 weak exon이 포함될 시간이 충분한 반면 빠르게 진행되면 그 놈의 속도가 exon을 인식할 시간을 낭낭히 안 주기 때문에 strong exon만 포함이 된다. 또한 intron이 긴 경우 intron을 제거하는데 time lag이 생기기 때문에 weak exon이 포함될 수 있게 된다.

Disease & Splicing
만일 이러한 Alternative splicing이 제대로 일어나지 않으면 어떻게 될까? 심한 경우에는 죽을 것이다. 간신히 살아남아서 진단받았다면 병에 걸릴 것이다. 세간에 알려진 splicing error로 인한 병을 알아보자.
Myotonic dystrophy
이 병에는 2개의 Splicing regulator protein, MBLN(Muscleblind, adult)과 CUGBP(CUG Binding protein, embryo)가 관여한다는 사실을 기억하고 시작해보자.
1. 발병 원인
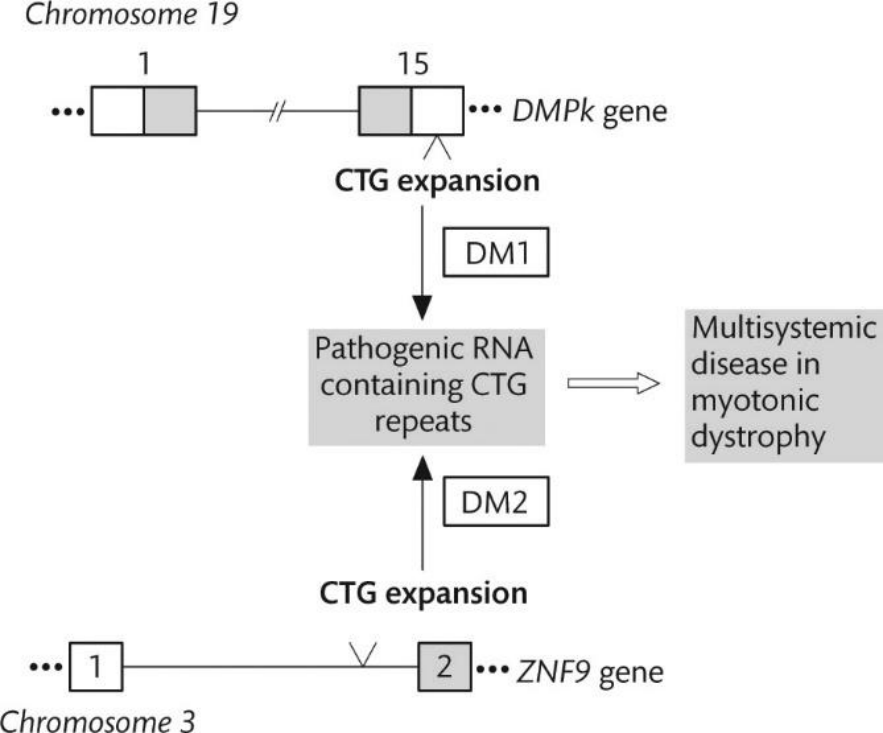 |
DM1은 DMPK gene의 3'UTR의 CTG expansion(5-37회 → 50~4000회)에 의해 발병된다. DM2는 ZFN9 gene의 CCTG expansion(75 → 11000회)에 의해서 발병된다. 두 경우 모두 UTR에서 생긴 변화기 때문에 생성되는 단백질 product는 동일하다. 다만 pathogenic mRNA가 생성될 뿐이다. 뒤에서 보겠지만 생성된 pathgenic RNA repeat은 embryonic splicing environment를 embryonic splicing pattern을 만듦으로써 성인에서 다양한 문제를 야기하게 된다. |
2. 기전
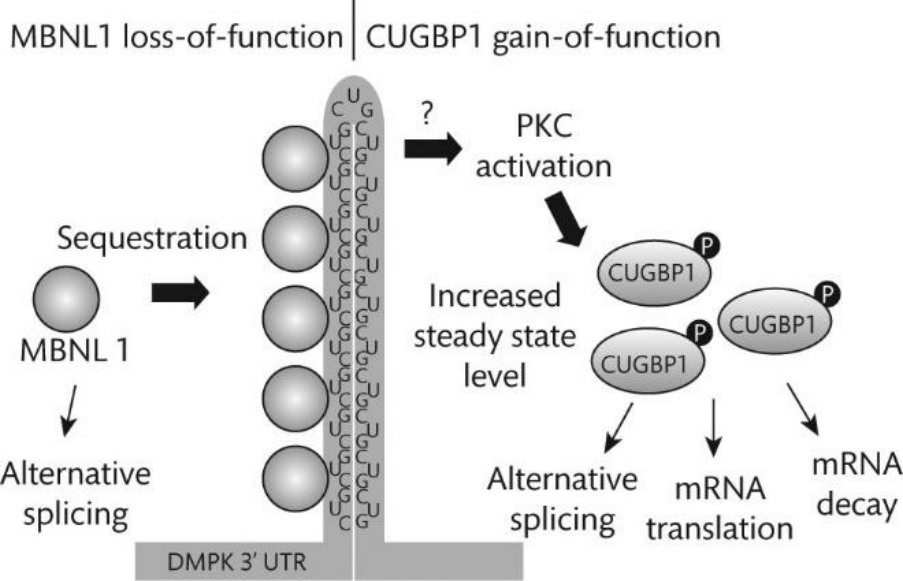 |
ㅇㅋ 그럼 늘어난 repeat이 어떤 문제를 야기하는지 알려주겠다. CUG repeat은 dsRNA를 형성한다. MBLN은 dsRNA에 붙어서 seqeuster 되는 반면 CUGBP는 본디 single strand CUG에 붙기 때문에 떠돌이 신세가 된다. 떠돌이 CUGBP는 PKC에 의해 activation되고 이것이 multisystemic 문제를 일으키게 되는 것이다. (따라서 mouse model은 MBLN 녹아웃, CUGBP over expression을 통해 만들어낼 수 있다.) |
3. 후폭풍
 |
 |
| 위와 같은 변화는 최소 20개 이상의 pre-mRNA의 splicing pattern을 변화시키게 된다. ① insulin receptor splicing 변화 -> insulin resistance ② Cl- channlel(ClC) -> poison exon이 포함되어 제대로 생성되지 못함 -> 근 수축 후 이완 불가 ③ cardiac troponin T -> splicing 안되던 exon5 포함 -> 심장 이상 |
|
NOVA
병...으로 소개하기 애매하다. 사실 여기서는 paraneoplastic disorder에 대해 언급하셨는데... 여튼 NOVA 1,2가 없으면motor neuron apoptosis가 일어나기 때문에 조기 사망에 이르게 되긴 한다.

NOVA1과 2는 alternative splicing으로 인해 생성된 isoform인데 둘은 서로를 보충할 수 없다.

여튼 NOVA는 원래 신경계에서 만들어지는 단백질이다. 근데 일부 암이 이 NOVA를 발현하고 있다. 암이 NOVA를 발현하면 암세포를 처치하기 위해 우리 몸의 면역계는 항체를 생성하게 되는데, 생성된 항체가 뇌를 공격하면 motor neuron의 파괴와 같은 무서운 일이 일어나게 된다. 이렇듯 암으로 인해서 새로이 발생하는 질병을 paraneoplastic disorder라고 칭한다. 한국말 번역이 웃기니까 꼭 찾아보면 좋겠다. 나만 웃기면 어떡하지.
급하게 끝내는 이유는 절대 화장실이 급해서가 아니다.